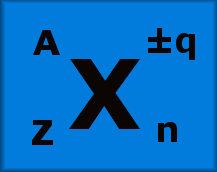La masa atómica es la masa de un átomo, más frecuentemente expresada en unidades de masa atómica unificada.1 La masa atómica puede ser considerada como la masa total de protones y neutrones (pues la masa de los electrones en el átomo es prácticamente despreciable) en un solo átomo (cuando el átomo no tiene movimiento). La masa atómica es algunas veces usada incorrectamente como un sinónimo de masa atómica relativa, masa atómica media y peso atómico; estos últimos difieren sutilmente de la masa atómica. La masa atómica está definida como la masa de un átomo, que sólo puede ser de un isótopo a la vez, y no es un promedio ponderado en las abundancias de los isótopos. En el caso de muchos elementos que tienen un isótopo dominante, la similitud/diferencia numérica real entre la masa atómica del isótopo más común y la masa atómica relativa o peso atómico estándar puede ser muy pequeña, tal que no afecta muchos cálculos bastos, pero tal error puede ser crítico cuando se consideran átomos individuales. Para elementos con más de un isótopo común, la diferencia puede llegar a ser de media unidad o más (por ejemplo, cloro). La masa atómica de un isótopo raro puede diferir de la masa atómica relativa o peso atómico estándar en varias unidades de masa.
que es el atomo
viernes, 16 de octubre de 2015
¿que es el numero atomico?
En física y química, el número atómico de un elemento químico es el número total de protones que tiene cada átomo de ese elemento. Se suele representar con la letra Z. Los átomos de diferentes elementos tienen distintos números de electrones y protones. Un átomo en su estado natural es neutro y tiene un número igual de electrones y protones. Un átomo de sodio (Na) tiene un número atómico 11; posee 11 electrones y 11 protones. Un átomo de magnesio (Mg), tiene número atómico 12, posee 12 electrones y 12 protones; y un átomo de uranio (U), que tiene número atómico 92, posee 92 electrones y 92 protones.
¿que es el electron?
El electrón (del griego clásico ἤλεκτρον ḗlektron ámbar), comúnmente representado por el símbolo: e−, es unapartícula subatómica con una carga eléctrica elemental negativa.12 Un electrón no tiene componentes o subestructura conocidos, en otras palabras, generalmente se define como una partícula elemental. En la teoría de cuerdas se dice que un electrón se encuentra formado por una subestructura (cuerdas).2 Tiene una masa que es aproximadamente 1836 veces menor con respecto a la del protón.13 El momento angular (espín) intrínseco del electrón es un valor semientero en unidades de ħ, lo que significa que es un fermión. Su antipartícula es denominada positrón: es idéntica excepto por el hecho de que tiene cargas —entre ellas, la eléctrica— de signo opuesto. Cuando un electrón colisiona con un positrón, las dos partículas pueden resultar totalmente aniquiladas y producir fotones de rayos gamma.
¿que es el neutron?
El neutrón es una partícula subatómica, un nucleón, sin carga neta, presente en el núcleo atómico de prácticamente todos los átomos, excepto el protio. Aunque se dice que el neutrón no tiene carga, en realidad está compuesto por tres partículas fundamentales cargadas llamadas quarks, cuyas cargas sumadas son cero. Por tanto, el neutrón es un barión neutro compuesto por dos quarks de tipo abajo, y un quark de tipo arriba.
¿que es un proton?
Experimentalmente, se observa el protón como estable, con un límite inferior en su vida media de unos 1035 años, aunque algunas teorías predicen que el protón puede desintegrarse en otras partículas. Originalmente se pensó que el protón era una partícula elemental pero desde los años 1970 existe una evidencia sólida de que es una partícula compuesta. Para la cromodinámica cuántica el protón es un
a partícula formada por la unión estable de tres quarks.
¿QUE ES UN ÁTOMO?
Un átomo es la unidad constituyente más pequeña de la materia ordinaria que tiene las propiedades de un elemento químico.1 Cada sólido, líquido, gas y plasma se compone de átomos neutros o ionizados. Los átomos son muy pequeños; los tamaños típicos son alrededor de 100 pm (diez mil millonésima parte de un metro).2 No obstante, los átomos no tienen límites bien definidos y hay diferentes formas de definir su tamaño que dan valores diferentes pero cercanos.
Los átomos son lo suficientemente pequeños para que la física clásica dé resultados notablemente incorrectos. A través del desarrollo de la física, los modelos atómicos han incorporado principios cuánticos para explicar y predeCada átomo se compone de un núcleo y uno o más electrones unidos al núcleo. El núcleo está compuesto de uno o másprotones y típicamente un número similar de neutrones (ninguno en el hidrógeno-1). Los protones y los neutrones son llamados nucleones. Más del 99,94 % de la masa del átomo está en el núcleo. Los protones tienen una carga eléctricapositiva, los electrones tienen una carga eléctrica negativa y los neutrones no tienen carga eléctrica. Si el número de protones y electrones son iguales, ese átomo es eléctricamente neutro. Si un átomo tiene más o menos electrones que protones, entonces tiene una carga global negativa o positiva, respectivamente, y se denomina ioncir mejor su comportamiento.
Suscribirse a:
Entradas (Atom)